①通式____________________;
②从F2→I2反应所需条件逐渐____;反应剧烈程度逐渐____;生成氢化物的稳定性逐渐____。
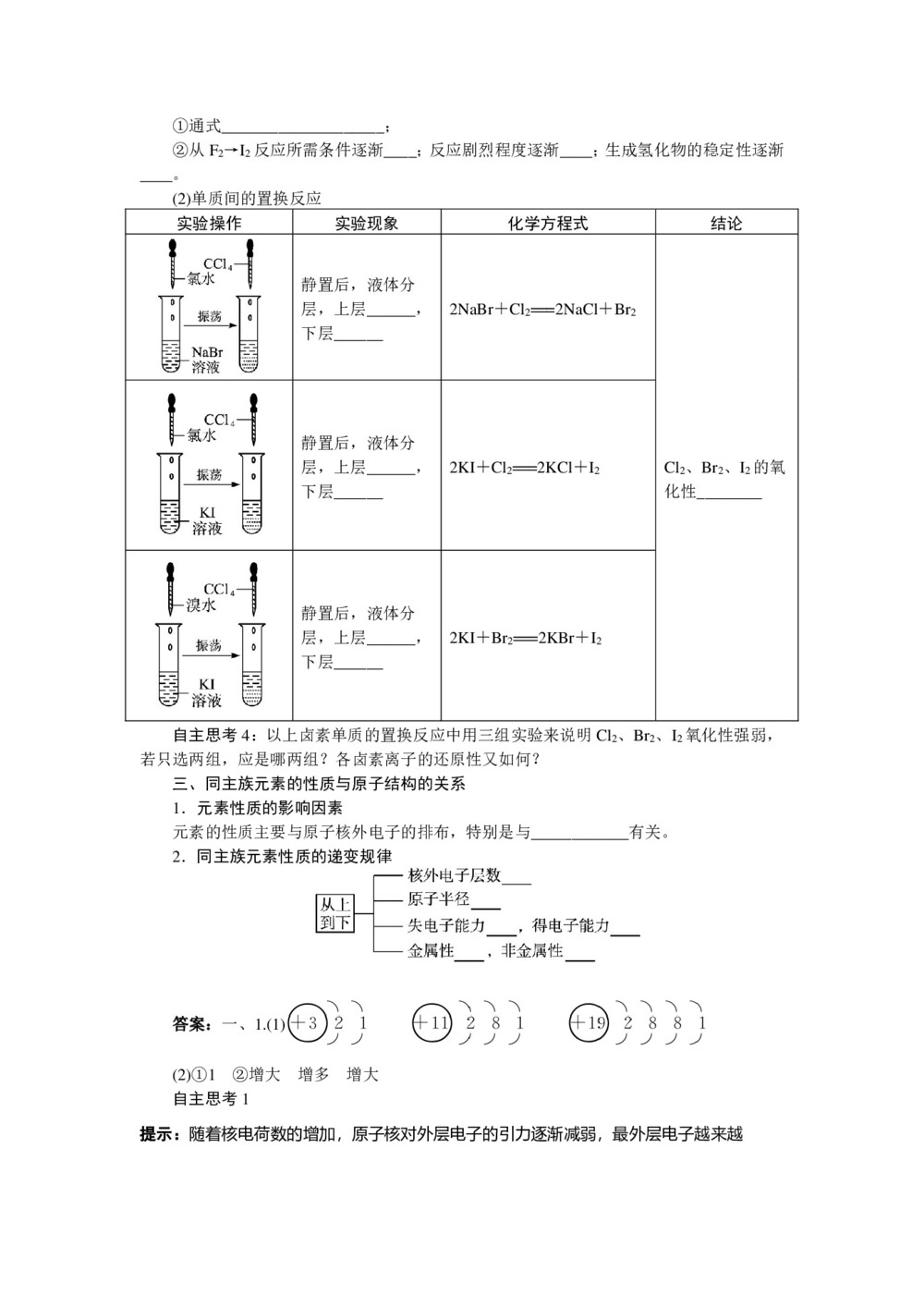
(2)单质间的置换反应
实验操作 实验现象 化学方程式 结论 静置后,液体分层,上层______,下层______ 2NaBr+Cl2===2NaCl+Br2 Cl2、Br2、I2的氧化性________ 静置后,液体分层,上层______,下层______ 2KI+Cl2===2KCl+I2 静置后,液体分层,上层______,下层______ 2KI+Br2===2KBr+I2 自主思考4:以上卤素单质的置换反应中用三组实验来说明Cl2、Br2、I2氧化性强弱,若只选两组,应是哪两组?各卤素离子的还原性又如何?
三、同主族元素的性质与原子结构的关系
1.元素性质的影响因素
元素的性质主要与原子核外电子的排布,特别是与____________有关。
2.同主族元素性质的递变规律
答案:一、1.(1)
(2)①1 ②增大 增多 增大
自主思考1
提示:随着核电荷数的增加,原子核对外层电子的引力逐渐减弱,最外层电子越来越
-
相关教案下载
- 12018-2019学年人教版必修2 第一章第一节元素周期表第1课时元素周期表和核素 学案
- 22018-2019学年人教版必修2 第一章第一节 元素周期表(第3课时) 学案
- 32018-2019学年人教版必修2 第一章第一节 元素周期表 教案
- 42018-2019学年鲁科版必修2 第一章第2节元素周期律和元素周期表 第2课时元素周期表 学案4
- 52018-2019学年人教版必修二 第1章 第一节 元素周期表第1课时 学案
- 62018-2019学年人教版必修2 第一章1.元素周期表 学案
- 72018-2019学年鲁科版必修2 第一章第2节元素周期律和元素周期表第2课时 教案
- 82018-2019学年鲁科版必修2 第一章第2节元素周期律和元素周期表第1课时 教案
- 92018-2019学年鲁科版必修2 第一章第2节元素周期律和元素周期表 学案5